Skillnad mellan versioner av "Fasjämvikter"
Per (Diskussion | bidrag) (Skapade sidan med 'En konsekvens av andra huvudsatsen är att vid jämvikt så är den kemiska potentialen för ett ämne lika i hela systemet, oavsett hur många faser som finns. Om den flytand...') |
Per (Diskussion | bidrag) |
||
| Rad 1: | Rad 1: | ||
En konsekvens av andra huvudsatsen är att vid jämvikt så är den kemiska potentialen för ett ämne lika i hela systemet, oavsett hur många faser som finns. Om den flytande och fasta fasen av ett ämne står i jämvikt med varandra är alltså den kemiska potentialen för ämnet lika i båda faserna. För att se detta, antag att den kemiska potentialen är högre i vätskefas än i fast fas, <math>\mu^l>\mu^s</math>. Vi tittar nu på processen då en liten mängd, <math>dn</math> överförs från vätska till fast fas. Summan av ändringen i Gibbs energi för vätskan och det fasta ämnet ges då av | En konsekvens av andra huvudsatsen är att vid jämvikt så är den kemiska potentialen för ett ämne lika i hela systemet, oavsett hur många faser som finns. Om den flytande och fasta fasen av ett ämne står i jämvikt med varandra är alltså den kemiska potentialen för ämnet lika i båda faserna. För att se detta, antag att den kemiska potentialen är högre i vätskefas än i fast fas, <math>\mu^l>\mu^s</math>. Vi tittar nu på processen då en liten mängd, <math>dn</math> överförs från vätska till fast fas. Summan av ändringen i Gibbs energi för vätskan och det fasta ämnet ges då av | ||
| − | :<math>dG=dG_l+dG_s=-\mu^l\,dn+\mu^s\,dn=(\mu^s-\mu^l)\,dn</math> | + | :<math>dG=dG_l+dG_s=-\mu^l\,dn+\mu^s\,dn=(\mu^s-\mu^l)\,dn<0</math> |
| + | där den sista olikheten följer av antagandet <math>\mu^l>\mu^s</math>. Processen, att molekyler överförs från vätskan till den fasta fasen, är alltså spontan eftersom den ger en negativ ändring i Gibbs energi. Jämvikt (d.v.s. att <math>dG=0</math>) kräver alltså att <math>\mu^l=\mu^s</math> | ||
| + | |||
| + | Antag nu att vi är vid en punkt (p, T) där jämvikt råder mellan två faser <math>\alpha</math> och <math>\beta</math>. Detta betyder alltså att vi befinner oss på någon av linjerna (fasgränserna) i det "vanliga" fasdiagrammet: | ||
| + | |||
| + | https://www.chemguide.co.uk/physical/phaseeqia/pdusual.gif | ||
| + | |||
| + | Enligt ovan gäller | ||
| + | |||
| + | :<math>\mu^\alpha(p,T)=\mu^\beta(p,T)\;\;\;\;\;</math> (1) | ||
| + | |||
| + | där vi förtydligat att den kemiska potentialen beror på tryck och temperatur. | ||
| + | |||
| + | Vi frågar oss nu på vilket sätt vi kan ändra ''p'' och ''T'' så att jämvikt fortfarande gäller, d.v.s. att vi "följer linjen" i fasdiagrammet. En sådan ändring måste ju uppfylla | ||
| + | |||
| + | :<math>d\mu^\alpha=d\mu^\beta</math> | ||
| + | |||
| + | eftersom (1) ska gälla både före och efter ändringen. Men vi vet från avsnittet om [[Gibbs_energi_och_kemisk_potential| tryck- och temperaturberoende för Gibbs energi]] att | ||
| + | |||
| + | :<math>d\mu^\alpha=V_m^\alpha\,dp - S_m^\alpha\,dT</math> | ||
| + | :<math>d\mu^\beta=V_m^\beta\,dp - S_m^\beta\,dT</math> | ||
| + | |||
| + | där vi använt att kemiska potentialen är detsamma som molär Gibbs energi för vardera fasen, eftersom varje fas här består av en enda komponent. Kombination av de tre senaste ekvationerna ger | ||
| + | |||
| + | :<math>V_m^\alpha\,dp - S_m^\alpha\,dT=V_m^\beta\,dp - S_m^\beta\,dT</math> | ||
| + | |||
| + | vilket kan förenklas till | ||
| + | |||
| + | :<math>\left(V_m^\alpha-V_m^\beta\right)\,dp = \left(S_m^\alpha- S_m^\beta\right)\,dT</math> | ||
| + | |||
| + | Detta är alltså det samband som måste gälla mellan tryck- och temperaturändringarna <math>dp</math> och <math>dT</math> för att jämvikten ska bibehållas. Om vi inför beteckningen <math>\Delta_{\alpha\rightarrow\beta}</math> för differensen mellan <math>\beta</math> och <math>\alpha</math> och "dividerar" differentialerna för att få en derivata, erhålls Clapeyrons ekvation: | ||
Versionen från 15 november 2017 kl. 11.20
En konsekvens av andra huvudsatsen är att vid jämvikt så är den kemiska potentialen för ett ämne lika i hela systemet, oavsett hur många faser som finns. Om den flytande och fasta fasen av ett ämne står i jämvikt med varandra är alltså den kemiska potentialen för ämnet lika i båda faserna. För att se detta, antag att den kemiska potentialen är högre i vätskefas än i fast fas, Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \mu^l>\mu^s} . Vi tittar nu på processen då en liten mängd, Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle dn} överförs från vätska till fast fas. Summan av ändringen i Gibbs energi för vätskan och det fasta ämnet ges då av
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle dG=dG_l+dG_s=-\mu^l\,dn+\mu^s\,dn=(\mu^s-\mu^l)\,dn<0}
där den sista olikheten följer av antagandet Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \mu^l>\mu^s} . Processen, att molekyler överförs från vätskan till den fasta fasen, är alltså spontan eftersom den ger en negativ ändring i Gibbs energi. Jämvikt (d.v.s. att Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle dG=0} ) kräver alltså att Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \mu^l=\mu^s}
Antag nu att vi är vid en punkt (p, T) där jämvikt råder mellan två faser Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \alpha} och Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \beta} . Detta betyder alltså att vi befinner oss på någon av linjerna (fasgränserna) i det "vanliga" fasdiagrammet:
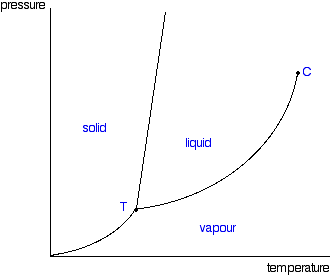
Enligt ovan gäller
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \mu^\alpha(p,T)=\mu^\beta(p,T)\;\;\;\;\;} (1)
där vi förtydligat att den kemiska potentialen beror på tryck och temperatur.
Vi frågar oss nu på vilket sätt vi kan ändra p och T så att jämvikt fortfarande gäller, d.v.s. att vi "följer linjen" i fasdiagrammet. En sådan ändring måste ju uppfylla
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle d\mu^\alpha=d\mu^\beta}
eftersom (1) ska gälla både före och efter ändringen. Men vi vet från avsnittet om tryck- och temperaturberoende för Gibbs energi att
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle d\mu^\alpha=V_m^\alpha\,dp - S_m^\alpha\,dT}
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle d\mu^\beta=V_m^\beta\,dp - S_m^\beta\,dT}
där vi använt att kemiska potentialen är detsamma som molär Gibbs energi för vardera fasen, eftersom varje fas här består av en enda komponent. Kombination av de tre senaste ekvationerna ger
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle V_m^\alpha\,dp - S_m^\alpha\,dT=V_m^\beta\,dp - S_m^\beta\,dT}
vilket kan förenklas till
- Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \left(V_m^\alpha-V_m^\beta\right)\,dp = \left(S_m^\alpha- S_m^\beta\right)\,dT}
Detta är alltså det samband som måste gälla mellan tryck- och temperaturändringarna Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle dp} och Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle dT} för att jämvikten ska bibehållas. Om vi inför beteckningen Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \Delta_{\alpha\rightarrow\beta}} för differensen mellan Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \beta} och Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://en.wikipedia.org/api/rest_v1/":): {\displaystyle \alpha} och "dividerar" differentialerna för att få en derivata, erhålls Clapeyrons ekvation: